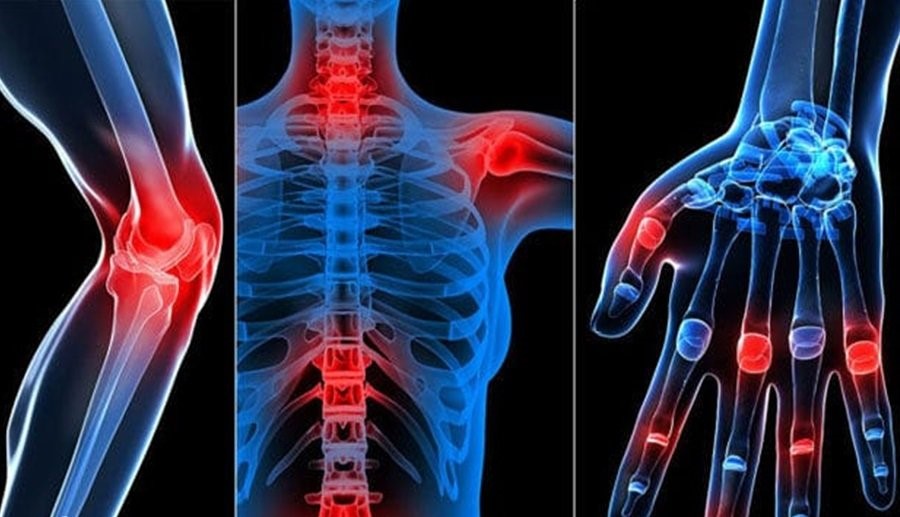
Viêm xương khớp là một trong những nguyên nhân hàng đầu gây tàn tật, ảnh hưởng gần 23.7% người trưởng thành ở Mỹ [1]. Thoái hóa khớp, một trong những bệnh lý thường gặp của viêm khớp, ảnh hưởng đến lầ 32.5 triệu người trưởng thành ở Mỹ. Những yếu tố nguy cơ dẫn đến tiến triển thoái hóa khớp gồm: tuổi (>50 tuổi), béo phì, tổn thương khớp gối (xương, sụn và tổn thương dây chằng), vận động khớp quá mức và giới tính (nữ) [2]
Thoái hóa khớp được đặc trưng bởi sự tiến triển nhanh chóng của việc thoái hóa sụn khớp, bắt đầu ở bàn tay, háng và khớp đầu gối. Trước đây thoái hóa khớp được biết đến như một bệnh không gây viêm, tuy nhiên các nghiên cứu mới đã chỉ ra rằng viêm màng hoạt dịch và viêm khớp chiếm tỉ lệ lớn ở những bệnh nhân thoái hóa khớp [3]. Bệnh nhân viêm xương khớp thường biểu hiện các triệu chứng như đau, cứng và sưng khớp, kèm theo hạn chế khả năng vận động. Cơn đau sâu, nhức thường biểu hiện khi cử động trong khi tình trạng cứng khớp và giảm phạm vi cử động sẽ cải thiện khi cử động. Trong viêm khớp gối và hông, các khớp bị sưng và cơ yếu xung quanh khớp bị ảnh hưởng góp phần gây mất ổn định, ảnh hưởng đến sự cân bằng tổng thể và tăng nguy cơ té ngã [2]
Hội Thấp khớp học Hoa Kỳ (The American College of Rheumatology - ACR), hợp tác với hiệp hội khớp học (Arthritis Foundation), cập nhật guideline về quản lý thoái hóa khớp tay, hông và gối vào năm 2019. Hiện tại vẫn chưa có thuốc đặc trị nào được chứng minh là có thể phòng ngừa hoặc giảm nhẹ sự tiến triển của thoái hóa khớp. Các liệu pháp sử dụng hoặc không sử dụng thuốc tập trung vào việc quản lý cơn đau, duy trì và cải thiện chất lượng sống và vận động khớp. Các triệu chứng được kiểm soát bằng việc sử dụng các thuốc không kê đơn hoặc kê đơn các thuốc giảm đau hoặc thuốc chống viêm, kết hợp với các liệu pháp không sử dụng thuốc như tập thể dục, vật lý trị liệu và giảm cân.
Các liệu pháp không sử dụng thuốc:
Tập thể dục (VD; đi bộ, bơi lội, rèn luyện thể lực), giảm cân, các chương trình quản lý sức khỏe có lợi cho tất cả các dạng thoái hóa khớp. Bệnh nhân được khuyến khích tham gia các hoạt động mà họ cảm thấy thoải mái, VD như thái cực quyền, môn võ thuật được cho là có lợi cho bệnh thoái hóa khớp đầu gối và khớp háng [4]. Giảm cân cũng giúp giảm áp lực lên đầu gối và khớp háng, có tiềm năng trong việc giảm tiến triển bệnh [4],[7]. Các thiết bị hỗ trợ, chẳng hạn như gậy, nẹp đầu gối hoặc dụng cụ chỉnh hình bàn tay, cũng có thể hữu ích cho một số bệnh nhân để giảm triệu chứng, cải thiện chức năng khớp và tăng chất lượng cuộc sống [4],[8],[9].
• NSAIDs
Guideline của Hội thấp khớp học Hoa kỳ khuyến khích mạnh mẽ việc sử dụng cái NSAIDs đường uống hoặc ngoài da cho bệnh nhân thoái hóa khớp.Cơ chế NSAIDs là ức chế enxyme cyclo-oxygenase, làm giảm sự tổng hợp prostaglandins and prostacyclins, làm giảm viêm, hạ sốt và giảm đau. Các phân tích tổng hợp (meta-analyses) gần đây cho thấy việc sử dụng NSAIDs đường uống làm giảm đau mạnh hơn so với acetaminophen, đặc biệt ở những bệnh nhân có cơ đau vừa đến nặng [10,[11]. Các thử nghiệm ngẫu nhiên so sánh (Comparator trials) cho thấy hiệu quả tương đường giữa NSAIDs đường uống và đường ngoài da ở bệnh nhân thoái hóa khớp gối và khớp tay [12-14]. Mặc dù các NSAIDs dạng bôi có hiệu quả với thoái hóa khớp tay, việc thường xuyên sử dụng bàn tay (VD: rửa tay hoặc đánh máy) hạn chế việc sử dụng loại thuốc này. Hiện nay, không có khuyến cáo nào cho việc sử dụng NSAIDs đường dùng ngoài cho thoái hóa khớp háng do hấp thu và hiệu quả không rõ ràng cũng như không đủ dữ liệu [4]. Một ưu điểm của NSAIDs tại chỗ là việc khu trú vùng giảm đau với sự hấp thu toàn thân tối thiểu, nhờ đó giảm nguy cơ tác dụng phụ toàn thân [12-14]. Do hiệu quả tương đương và khả năng dung nạp được cải thiện, NSAID tại chỗ được khuyến cáo là phương pháp điều trị đầu tay so với NSAID đường uống cho thoái hóa khớp đầu gối [4]
Đối với NSAIDs đường uống, diclofenac hoạt chất duy nhất có dạng bào chế tại chỗ. Diclofenac được bôi tại chỗ 2-4 lần mỗi ngày tại vị trí đau. Cần lưu ý cho bệnh nhân rằng các NSAIDs tại chỗ không cho tác dụng giảm đau tức thời, thường sẽ mất khoảng ít nhất 1-2 tuần để thấy rõ tác dụng.
Trong khi NSAIDs đường uống đã được chứng minh là có hiệu quả trong việc quản lý thoái hóa khớp, loại thuốc này thường đi kèm với các tác dụng phụ và chống chỉ định, làm giảm khả năng sử dụng ở một số quần thể bệnh nhân. Các tác dụng phụ nghiêm trọng bao gồm tăng nguy cơ biến cố tim mạch (VD: nhồi máu cơ tim, đột quỵ), suy giảm chức năng thận, chảy máu đường tiêu hóa và giữ nước trong cơ thể. Nên thận trọng khi sử dụng NSAIDs đường uống với bệnh nhân cao tuổi và những người có tiền sử suy thận, suy giảm chức năng gan, có các biến có tim mạch(VD: tăng huyết áp, đột quỵ, suy tim,..) hoặc loét đường tiêu hóa, người đang sửu dụng thuốc chống đông hoặc thuốc chống kết tập tiểu cầu [15-17]. Bệnh nhân thoái hóa khớp có nguy cơ cao về biến cố tim mạch hoặc đường tiêu hóa nên được kiểm soát khi sử dụng NSAIDs đường uống sau khi cẩn trọng chọn được hoạt chất cụ thể và theo dõi chặt chẽ. Tốt nhất ở những bệnh nhân này nên tránh sử dụng NSAIDs đường uống. Loại thuốc này cũng nên được sử dụng ở liều thấp nhất có hiệu quả và tỏng thời gian ngắn nhất có thể để hạn chê các tác dụng phụ. Ngược lại, các NSAIDs tác dụng tại chỗ khi được sử dụng ở liều khuyến cáo có ít tác dụng phụ toàn thân nên thường được xem là an toàn cho đa số bệnh nhân.
• Acetaminophen
Acetaminophen từ lâu đã được xem như là một lựa chọn cho thoái hóa khớp háng và gối không viêm, và tiếp tục được khuyến cáo ở những bệnh nhân không thể sử dụng NSAIDs [4],[5]. Mặc dù acetaminophen được cho là có lợi cho các triệu chứng viêm khớp thông qua tác dụng giảm đau và chống viêm yếu, các phân tích tổng hợp đã xác định mức độ hiệu quả từ thấp đến tối thiểu đối với tình trạng đau và chức năng [11],[18]. Một nghiên cứu tổng quan hệ thống (systematic review) bởi Leopoldino và cộng sự so sánh hiệu quả của acetaminophen với giả dược trong thoái hóa khớp gối và háng kết luận rằng có nhiều bằng chứng cho thấy paracetamol có tác dụng giảm đau tối thiểu [18]. Mặc dù paracetamol dung nạp tốt và an toàn khi dùng ở liều khuyến cáo, bệnh nhân với bệnh gan cấp hoặc mạn tính nên tránh sử dụng paracetamol.
• Duloxetine
Duloxetine được khuyến cáo tùy điều kiện cho thoái hóa khớp bàn tay, gối và háng và có thể thay thế liệu pháp sử dụng NSAIDs [4]. Duloxetine chủ yếu ức chế tái hấp thu serotonin và norepinephrine đồng thời ức chế yếu tái hấp thu Dopamine, từ đó làm giảm tín hiệu đau ngoại biên [17],[19]. Duloxetine đã được chứng minh là có lợi ích đáng kể về mặt chức năng và giảm đau ở bệnh nhân thoái hóa khớp gối khi so sánh với bệnh nhân sử dụng NSAIDs [20] Duloxetine nên được khởi đầu với liều 30mg 1 lần mỗi ngày trong tuần đầu tiên, sau đó tăng liều lên tối đa 60mg một ngày [17]. Tác dụng phụ thường gặp bao gồm đau đầu, táo bón và khô miệng [17].
• Tramadol và các opioid khác
Tramadol được khuyến cáo có điều kiện ở những bệnh nhân viêm khớp không thể dùng NSAID đường uống hoặc tiếp tục gặp các triệu chứng khi sử dụng NSAID. Mặc dù tác dụng giảm đau của tramadol cho thấy sự giảm nhẹ các triệu chứng viêm khi so sánh với giả dược, chúng thường kèm theo các tác dụng không mong muốn như táo bón, chóng mặt và đau đầu [17],[21]. Các opioid khác không phải tramadol không được khuyến cáo vì tăng nguy cơ của các tác dụng phụ như gây nghiện và lệ thuộc thuốc, tuy nhiên việc lựa chọn loại thuốc này vẫn có thể xem xét neeys tramadol không đủ để giảm đau [4]
• Capsaicin
Capsaicin tại chỗ được khuyến cáo có điều kiện cho thoái hóa khớp gối và nên được cân nhắc như một lựa chọn thay thế NSAIDs tại chỗ trước khi chuyển sang các thuốc đường uống [14]. Capsaicin, dẫn xuất của quả ớt, được cho là có tác dụng giảm đau bằng cách kích thích thụ thể TRPV1(transient receptor potential vanilloid 1), ban đầu gây cảm giác nóng sau đó là tác dụng giảm đau [17]. Khi so sánh với giả dược, capsaicin được cho là có tác dụng giảm đau tốt hơn cho bệnh thoái hóa khớp đầu gối và bàn tay [22]. Tác dụng phụ chính thường gặp là cảm giác bỏng rát khi bôi và kích ứng da. Thuốc này không được khuyến cáo ở bệnh nhân thoái hóa khớp ở tay do nguy cơ gây nguy hiểm khi tay tiếp xúc với mắt hoặc miệng.
• Glucosamine và Chondroitin
Mặc dù glucosamine và chondronitin được sử dụng như thuốc thảo dược để điều trị triệu chứng thoái hóa khớp rất lâu trước đây, những nghiên cứu chỉ ra những tác dụng có lợi rất nhỏ [22],[23]. Guideline của Hội thấp khớp học Hoa Kỳ không khuyến cáo sử dụng chondroitin và glucosamine cho thoái khóa khớp háng và khớp gối, trong khi chondroitin được khuyến cáo có điều kiện ở bệnh nhân thoái hóa khớp bàn tay [4]. Những hoạt chất này thúc đẩy sự sản sinh sụn cũng như ngăn ngừa thoái hóa sụn khớp [25]. Một phân tích tổng hợp (meta-analysis) bởi Wandel và cộng sự cho thấy không hoạt chất nào trong 2 loại thuốc kể trên dù ở dạng phối hợp hay đơn lẻ có thể cải thiện cơn đau khi so sánh với giả dược [23]. Đối với bệnh nhân thoái hóa khớp bàn tay, một nghiên cứu bởi Gabay và cộng sự chỉ ra răng chondroitin 800mg khi so sánh với giả dược làm giảm đáng kể cơn đau khi sử dụng thang điểm đau VAS (Visual Analog Scale) và cải thiện thời gian cứng khớp buổi sáng cũng như chức năng khớp; tuy nhiên không có nghiên cứ nào lặp lại kết quả này [24]. Có thể lưu ý rằng có sự khác biệt đáng kể về công thức và nồng độ được sử dụng, điều này có thể góp phần tạo ra hiệu quả trái ngược nhau được tìm thấy trong tài liệu về các sản phẩm này.
• Tiêm nội khớp
Tiêm nội khớp, đặc biệt là glucocorticoid và hyaluronic acid, thường được coi là lựa chọn điều trị cuối cùng do tính chất xâm lấn và tác dụng phụ liên quan đến trị liệu [4].Một nghiên cứu vào đầu năm 2000 chỉ ra rằng việc tiêm nội khớp glucocorticoid cho thấy hiệu quả và độ an toàn lâu dài khi so sánh với giả dược trong điều trị thoái hóa khớp gối có triệu chứng [26]. Ngược lại, một nghiên cứu gần đây cho thấy sự giảm sụn khớp, và nguy cơ làm nặng cơn đau và tiến triển thoái hóa khớp khi sử dụng trong thời gian dài [27]. Tại thời điểm này, do bằng chứng còn hạn chế và mâu thuẫn ủng hộ việc sử dụng chúng để quản lý viêm khớp, nên tiêm nội khớp bằng axit hyaluronic được khuyến cáo có điều kiện để điều trị viêm khớp ở tay và đầu gối và được khuyến cáo trong điều trị viêm khớp háng [4],[28].
Tài liệu tham khảo
1. Theis K, Murphy L, Guglielmo D, et al. Prevalence of arthritis and arthritis-attributable activity limitation–United States, 2016–2018. MMWR Morb Mortal Wkly Rep. 2021;70(40):1401-1407.
2. Arthritis Foundation. Osteoarthritis. www.arthritis.org/diseases/osteoarthritis. Accessed December 10, 2022.
3. Sokolove J, Lepus CM. Role of inflammation in the pathogenenesis of osteoarthritis: latest findings and interpretations. Ther Adv Musculoskelet Dis. 2013;5(2):77-94.
4. Kolasinski SL, Neogi T, Hochberg MC, et al. 2019 American College of Rheumatology/Arthritis Foundation Guideline for the Management of Osteoarthritis of the Hand, Hip, and Knee [published correction appears in Arthritis Rheumatol. 2021;73(5):764]. Arthritis Rheumatol. 2020;72(2):220-233.
5. Hochberg MC, Altman RD, April KT, et al. American College of Rheumatology 2012 recommendations for the use of nonpharma¬cologic and pharmacologic therapies in osteoarthritis of the hand, hip, and knee. Arthritis Care Res (Hoboken). 2012;64(4):465-474.
6. CDC. Osteoarthritis (OA). July 27, 2020. www.cdc.gov/arthritis/basics/osteoarthritis.htm. Accessed December 10, 2022.
7. Vincent HK, Heywood K, Connelly J, Hurley RW. Obesity and weight loss in the treatment and prevention of osteoarthritis. PM R. 2012;4(5 suppl):S59-S67.
8. Jones A, Silva PG, Silva AC, et al. Evaluation of immediate impact of cane use on energy expenditure during gait in patients with knee osteoarthritis. Gait Posture. 2012;35(3):435-439.
9. Raja K, Dewan N. Efficacy of knee braces and foot orthoses in conservative management of knee osteoarthritis. Am J Phys Med Rehabil. 2011;90(3):247-262.
10. Towheed TE, Maxwell L, Judd MG, et al. Acetaminophen for osteoarthritis. Cochrane Database Syst Rev. 2006;2006(1):CD004257.
11. Da Costa BR, Reichenbach S, Keller N, et al. Effectiveness of non-steroidal anti-inflammatory drugs for the treatment of pain in knee and hip osteoarthritis: a network meta-analysis. Lancet. 2017;390:e21-e33.
12. Derry S, Conaghan P, Da Silva JAP, et al. Topical NSAIDs for chronic musculoskeletal pain in adults. Cochrane Database Syst Rev. 2016;4(4):CD007400.
13. Simon LS, Grierson LM, Naseer Z, et al. Efficacy and safety of topical diclofenac containing dimethyl sulfoxide (DMSO) compared with those of topical placebo, DMSO vehicle and oral diclofenac for knee osteoarthritis. Pain. 2009;143(3):238-245.
14. Rannou F, Pelletier JP, Martel-Pelletier J. Efficacy and safety of topical NSAIDs in the management of osteoarthritis: evidence from real-life setting trials and surveys. Semin Arthritis Rheum. 2016;45(4 suppl):S18-S21.
15. Bello AE, Holt RJ. Cardiovascular risk with non-steroidal anti-inflammatory drugs: clinical implications. Drug Saf. 2014;37(11): 897-902.
16. Bhala N, Emberson J, Merhi A, et al; Coxib and traditional NSAID Trialists’ (CNT) Collaboration. Vascular and upper gastrointestinal effects of non-steroidal anti-inflammatory drugs: meta-analyses of individual participant data from randomized trials. Lancet. 2013;382:769-779.
17. Lexi-Drugs. Tramadol. Updated July 27, 2015. Hudson, OH: Lexicomp, 2015. http://online.lexi.com/. Accessed December 3, 2022.
18. Leopoldino AO, Machado GC, Ferreira PH, et al. Paracetamol versus placebo for knee and hip osteoarthritis. Cochrane Database Syst Rev. 2019;2(2):CD013273.
19. Chen B, Duan J, Wen S, et al. An updated systematic review and meta-analysis of duloxetine for knee osteoarthritis. Pain. 2021;37(11):852-862.
20. Osani MC, Bannuru RR. Efficacy and safety of duloxetine in osteoarthritis: a systematic review and meta-analysis. Korean J Intern Med. 2019;34(5):966-973.
21. Toupin April K, Bisaillon J, Welch V, et al. Tramadol for osteoarthritis. Cochrane Database Syst Rev. 2019;5(5):CD005522.
22. Persson MSM, Stocks J, Walsh DA, et al. The relative efficacy of topical non-steroidal anti-inflammatory drugs and capsaicin in osteoarthritis: a network meta-analysis of randomised controlled trials. Osteoarthritis Cartilage. 2018;26(12):1575-1582.
23. Wandel S, Juni P, Tendal B, et al. Effects of glucosamine, chondroitin, or placebo in patients with osteoarthritis of hip or knee: network meta-analysis. BMJ. 2010;341:c4675.
24. Gabay C, Medinger-Sadowski C, Gascon D, et al. Symptomatic effects of chondroitin 4 and chondroitin 6 sulfate on hand osteoarthritis: a randomized, double-blind, placebo-controlled clinical trial at a single center. Arthritis Rheum. 2011;63(11):3383-3391.
25. Natural Medicines. Somerville, MA: Therapeutic Research Center. https://naturalmedicines.therapeuticresearch.com. Accessed December 13, 2022.
26. Raynauld JP, Buckland-Wright C, Ward R, et al. Safety and efficacy of long-term intraarticular steroid injections in osteoarthritis of the knee. Arthritis Rheum. 2003;48(2):370-377.
27. McAlindon TE, LaValley MP, Harvey WF, et al. Effect of intra-articular triamcinolone vs saline on knee cartilage volume and pain in patients with knee osteoarthritis. JAMA. 2017;317(19):1967-1975.
28. Ayhan E, Kesmezacar H, Akgun I. Intraarticular injections (corticosteroid, hyaluronic acid, platelet rich plasma) for the knee osteoarthritis. World J Orthop. 2014;5(3):351-361.